Глицеринът получава физични и химични свойства. Физични и химични свойства на глицерина и неговото приложение. Как се получава глицеринът?
Добър ден приятели! Днес ще говорим за невероятно вещество - глицерин.
Глицеринът е доста често срещано вещество. Може да се намери в състава на много лекарства, мехлеми, кремове,сапуни дори в шампоани.
Как се добива и къде се използва?
Основната част от глицерина се получава като страничен продукт при осапунването на мазнините.
Обхватът на глицерина е обширен. Използва се в много индустрии: медицинска, тютюнева, текстилна, хартиена, бояджийска и лакова промишленост, в производството на битова химия, електроника, радиотехника и др.
Глицеринът, чиито свойства са толкова разнообразни, се използва широко у дома. Например, при лечение на кожни заболявания и изгаряния, той е ефективен при кашлица, има слабително свойство и е най-простият овлажнител.
Най-често срещаните рецепти за използване на глицерин у дома:
Glycerin Physico Химични свойствана това невероятно вещество, нека разгледаме по-подробно.
Химични свойства
Химичните свойства на глицерина са същите като тези на другите многовалентни алкохоли. И това не са всички свойства на глицерина. Едно от предимствата на използването на глицерин е неговата ниска цена и наличност, така че неговите уникални свойства могат лесно да се използват в. Глицеринът може да бъде закупен в аптеки или онлайн магазини.
Нека да разгледаме основните свойства на глицерина, които ще бъдат полезни вприложение .
Физически Имоти
 Медицинският глицерин е безцветна вискозна течност, без мирис и сладък вкус. Ето защо е получил името си ("гликос" на гръцки - сладък). Глицеринът е нетоксичен, разтворим във вода във всякакви количества, добър разтворител е за неорганични соли, алкални, моно- и дизахариди.
Медицинският глицерин е безцветна вискозна течност, без мирис и сладък вкус. Ето защо е получил името си ("гликос" на гръцки - сладък). Глицеринът е нетоксичен, разтворим във вода във всякакви количества, добър разтворител е за неорганични соли, алкални, моно- и дизахариди.
Хигроскопичност- способността на веществата да абсорбират влагата от въздуха
Глицерин в чиста формахигроскопичен, т.е. той е в състояние да отнеме влагата (абсорбира вода до 40% от теглото си), така че може да изсуши кожата. Но в количеството (процентът обикновено не надвишава 7%), в което се използва в козметологията, има обратен (овлажняващ) ефект. Глицеринът намира широко приложение като овлажнител и омекотител.
След използване на козметичен продукт с добавка на глицерин кожата ви ще бъде овлажнена, омекотена, гладка и еластична. В чистата си форма, напротив, ще изсуши кожата, поради което не се използва отделно в козметологията.

Глицеринът извлича влагата от околния въздух и насища кожата ни с нея, образувайки влажен филм върху повърхността на кожата. Ами ако въздухът е сух? В този случай глицеринът ще вземе влагата от слоевете на кожата, изсушавайки я.
Ето защо е необходимо да се придържате към някои правила, когато използвате глицерин в козметиката.:
не използвайте чист глицерин и не използвайте продукти с глицерин в сух климат.
Разтворимост
Глицеринът е в състояние да разтваря различни органични и не органична материя: йод, алкали, различни соли, захари и др. Подобрява почистващата сила на почистващите продукти. Той е чест гост в състава на почистващите препарати за стъкло, ще помогне за премахване на мазни петна.
Пластмаса
Глицеринът подобрява детергентния компонентсапун и му придава пластичност. Благодарение на това работата със сапун основа с глицеринпо-лесно и повече възможности за реализиране на идеи. Същото свойство на глицерина се използва за маскиране на ниско качество. Лошата водка, ако към нея се добави глицерин, не замръзва на студено, а става малко вискозна, като висококачествен аналог. Ето защо, ако срещнете глицерин в състава на водка, направете съответните изводи.

антисептик
Глицеринът е отличен антисептик. Вероятно сте забелязали, че при нанасяне на крем с добавка на глицерин раните заздравяват по-бързо.
Често се използва комбинация от няколко свойства на глицерина наведнъж. Например, глицеринът се използва като омекотител в производството на тъкани и кожа поради своята пластичност и хигроскопичност. У дома може да помогне за връщането.
За козметични цели глицеринът е важен при производството на омекотяващи, овлажняващи и почистващи маски, лосиони, кремове. Като всеки естествен продукт, той се приема по-добре от кожата, отколкото синтетичен продукт.
Глицеринови маски полезно не  само когато се грижи за кожата на лицето и ръцете, но също така ще служи като отлична услуга, когато
само когато се грижи за кожата на лицето и ръцете, но също така ще служи като отлична услуга, когато
Многовалентни алкохоли- Това са органични съединения, чиито молекули съдържат две или повече хидроксилни групи, свързани с въглеводороден радикал.
ОН групите в поливалентните алкохоли са разположени при различни въглеродни атоми:
Съединенията с две ОН групи при един въглероден атом са нестабилни. Те отделят водата и се превръщат в алдехиди:
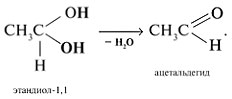
Съединения с две ОН групи при съседни въглеродни атоми се наричат гликоли (или диоли).
Касова бележка
Гликолите се получават чрез окисление на алкени във водна среда. Например, под действието на калиев перманганат или атмосферен кислород в присъствието на сребърен катализатор, алкените се превръщат в двувалентни алкохоли:

Друг начин за получаване на поливалентни алкохоли е хидролизата на халогенни производни на въглеводороди:
При производството глицеринът се получава по схемата:

Физически свойства
Етиленгликолът и глицеринът са безцветни вискозни течности със сладък вкус (от гръцки - сладък). Разтворимостта във вода е неограничена. Точки на кипене на етилен гликол - 197,2 °C, глицерин - 290 °C. Етилен гликолът е отрова.
Химични свойства
Етиленгликолът и глицеринът са подобни на едновалентните алкохоли.
Така те реагират с активни метали:

Многовалентни алкохоли в реакция с водородни халогенидиобменят една или повече ОН хидроксилни групи за халогенни атоми:

Глицеринът взаимодейства с азотна киселиназа образуване на естери. В зависимост от условията на реакцията (моларно съотношение на реагентите, концентрация на катализатора - сярна киселина и температура) се получават моно-, ди- и тринитроглицериди:

Качествена реакция на многовалентни алкохоли, което прави възможно разграничаването на съединения от този клас, е взаимодействието с прясно приготвен меден (II) хидроксид. В алкална среда с достатъчна концентрация на глицерол, синята утайка Cu (OH) 2 се разтваря, за да образува яркосин разтвор - меден (II) гликолат:

 |
УПРАЖНЕНИЯ.
1. Подчертайте структурните формули на поливалентните алкохоли:
СlCH 2 CH 2 Cl, HOS 3 H 7, NOCH 2 CH 2 OH, C 2 H 6 O 2, 
NOCH 2 COOH, NOCH 2 CH 2 CH 2 OH, CH 3 OCH 2 CH 2 OH.
2. Съставете техните структурни формули по имената на веществата:
а) етандиол-1,2; б) етилен гликол; в) пропандиол-1.2 г) пропандиол-1.3;
д) глицерин; е) бутантриол-1,2,4.
3.
Напишете уравненията на реакцията за получаване на етиленгликол от:
а) етилен; б) 1,2-дибромоетан.
4. Посочете пет области на приложение на поливалентните алкохоли (етиленгликол и глицерол).
5. Напишете реакционни уравнения за верига от химични трансформации, назовете органични вещества:
6.
Направете верига от химични трансформации, за да получите двувалентен алкохол
CH 3 CHONCH 2 OH от алкан C3H8. Използвайте схема:
наситен въглеводород монохало-въглеводород ненаситен въглеводород дихало-въглеводород двувалентен алкохол.
Отговори на упражнения към тема 2
Урок 20
1. Структурните формули на поливалентните алкохоли са подчертани:
2. Структурни формули, съставени от имената на веществата:
3. Реакции за получаване на етиленгликол:

4. Пет области на приложение на поливалентните алкохоли.
етиленов гликол(EG) - в антифриз, 66% EG замръзва при -60 ° C;
в синтеза на лавсан [–CH 2 CH 2 O(O)CC(O)O–] н;
разтворител ( Tт.к. = 198 °С).
Глицерол- в парфюмерията, козметиката, медицината - разтворител, компонент на мехлеми;
за производство на тринитроглицерин – експлозив и лекарство, което разширява кръвоносните съдове.
5. Реакции за верига от химични трансформации:

6. Веригата от химични превръщания на C 3 H 8 алкан в пропилей гликол CH 3 CHOHCH 2 OH чрез междинни вещества от дадени класове.
Глицеринът или, според международната номенклатура, пропантриол -1,2,3, е сложно вещество, което принадлежи към поливалентните алкохоли, или по-скоро е тривалентен алкохол, т.к. има 3 хидроксилни групи - ОН. Химичните свойства на глицерина са подобни на тези на глицерола, но са по-изразени поради факта, че има повече хидроксилни групи и те взаимно си влияят.
Глицеринът, подобно на алкохолите с една хидроксилна група, е силно разтворим във вода. Това, може да се каже, също е качествена реакция към глицерол, тъй като той се разтваря във вода в почти всяко съотношение. Това свойство се използва при производството на антифризи - течности, които не замръзват и охлаждат двигателите на автомобили и самолети.
Глицеринът също взаимодейства с калиев перманганат. Това е качествена реакция на глицерин, който също се нарича вулкан Шееле. За да го извършите, е необходимо да добавите 1-2 капки безводен глицерин към праха от калиев перманганат, който се изсипва под формата на пързалка с вдлъбнатина в порцеланова купа. След минута сместа се запалва спонтанно.По време на реакцията се отделя голямо количество топлина и горещите частици от продуктите на реакцията и водните пари се разлитат. Тази реакция е редокс.

Глицеринът е хигроскопичен, т.е. способни да задържат влагата. На това свойство се основава следната качествена реакция към глицерина. Извършва се в абсорбатор. За да го извършите, изсипете около 1 cm3 кристален калиев хидроген сулфат (KHSO4) в чиста, суха епруветка. Добавете 1-2 капки глицерин, след което загрейте, докато се появи остра миризма. Калиевият хидрогенсулфат действа тук като водопоглъщащо вещество, което започва да се проявява при нагряване. Глицеринът, губейки вода, се превръща в ненаситено съединение - акролеин, което има остра неприятна миризма. C3H5(OH)3 - H2C=CH-CHO + 2 H2O.
Реакцията на глицерол с меден хидроксид е качествена и служи за определяне не само на глицерол, но и на други, за да се осъществи първоначално е необходимо да се приготви пресен разтвор на меден (II) хидроксид. За да направим това, добавяме и получаваме меден (II) хидроксид, който образува синя утайка. Добавяме няколко капки глицерин към тази епруветка с утайка и забелязваме, че утайката е изчезнала и разтворът е придобил син цвят.

Полученият комплекс се нарича меден алкохолат или глицерат. Използва се качествена реакция на глицерин с меден (II) хидроксид, ако глицеринът е в чиста форма или във воден разтвор. За извършване на такива реакции, при които глицеролът е с примеси, е необходимо предварително да се пречисти от тях.
Качествените реакции на глицерина помагат да се открие във всяка среда. Това се използва активно за определяне на глицерол в храни, козметика, парфюми, лекарства и антифризи.
Глицеринът е вискозна, безцветна течност с леко сладък вкус. Глицеринът е безопасен за консумация от човека. Намира се в много продукти, от бонбони до паста за зъби. Широкото разпространение на глицерина във фармацевтичната, сладкарската, козметичната и други индустрии се дължи на неговите свойства.
Свойства на глицерина
Глицеринът е органично съединение. Глицеринът се получава от растителни и животински масла. Глицеринът е силно разтворим във вода и алкохол. От друга страна, много вещества, които са слабо разтворими в алкохол и вода, могат да се разтворят в глицерин. От това можем да заключим, че глицеринът е добър разтворител.
Глицеринът е 1500 пъти по-вискозен от водата. Тази вискозна прозрачна течност има висока точка на кипене и практически не замръзва.
Тъй като глицеринът не реагира с масла и следователно е по-устойчив на окисляване от минералните вещества, глицеринът може да се използва като смазка. Може да се използва за смазване на части и механични части, които са изложени на бензен или бензин, тъй като те не се разтварят в глицерин.
Прозрачният цвят позволява да се използва в много индустрии, тъй като не влияе по никакъв начин на цвета на крайния продукт.
Глицеринът е хигроскопична течност. Ако капнете чист глицерин върху езика си, можете да се изгорите. Но когато се разрежда с вода, глицеринът овлажнява добре кожата.
Как се получава глицеринът?
Глицеринът е страничен продукт при производството на сапун. До 1889 г. те не знаеха как да възстановят в процеса на производство на сапун.
През 1889 г. е намерен начин за отделяне на глицерин от сапун. Основната му употреба по това време е производството на нитроглицерин, от който се прави динамит.
Процесът на отстраняване на глицерин от сапун е доста сложен. Сапунът се прави от растителни или животински мазнини, които вече съдържат глицерин в състава си от 7 до 13 процента. Когато мазнините реагират с алкали, се получава сапун. Но глицеринът е в самия сапун.
При добавяне на сол сапунът се отделя и в останалия течен остатък има глицерин и други примеси. След това глицеринът се отделя чрез хидролиза и допълнително се пречиства чрез филтриране през въглеродни филтри или по други методи. 
Състав на глицерин
Глицеринът има молекулярна формула C3H5 (OH) 3. Състои се от верига от три въглеродни атома, така че всеки въглероден атом е свързан с водороден атом (H+) и хидроксилна група (OH-). Всеки от двата крайни въглерода има допълнителен водород, така че и трите въглерода имат общо четири връзки. Въглеродът има валентност четири, което означава, че има тенденция да образува четири връзки.
Мастните киселини са клас съединения, които по същество представляват дълга верига от въглеродни атоми, свързани с различни комбинации от кислородни и водородни атоми. Всяка молекула на мастна киселина завършва с въглероден атом, който образува двойна връзка с кислороден атом и единична връзка с хидроксилна група. Тази група има формула COOH- и се нарича карбоксилна група.
Триглицеридите са естери на глицерол с дълговерижни карбоксилни киселини.
Приложение на глицерин
Глицеринът се използва в много области, включително медицината.
хранително-вкусовата промишленост
В храните и напитките глицеринът служи като овлажнител, разтворител и подсладител. Използва се за производството на нискокалорични продукти като заместител на мазнините, като сгъстител в ликьори.
Глицеринът се използва и като заместител на захарта. За разлика от захарта, той инхибира растежа на бактериите. Освен това глицеринът има по-нисък гликемичен индекс. В хранителните продукти глицеринът се обозначава като Е 422.
Глицерин в медицината
В медицината глицеринът се използва в сиропи за кашлица, еликсири и отхрачващи средства. Използва се в производството на пасти за зъби, води за уста.
В твърди лекарства като таблетки, глицеролът се използва като водозадържащ агент.
Глицеринът има слабителни свойства и се използва като слабително в супозитории или под формата на микроклизми.
Глицеринът, смесен по-често с плодов сок за намаляване на сладкия вкус, може да се приема като първо спешно лечение за повишено очно налягане. Бързо намалява вътреочното налягане.
Глицеринът има диуретичен ефект, което означава, че може да допринесе за дехидратация и не трябва да се използва редовно. 
Глицерин в козметиката
В козметиката глицеринът се използва като овлажняваща съставка в продукти за грижа за кожата, кремове за бръснене и други продукти за лична хигиена.
Глицеринът е основната съставка на глицериновия сапун. Този вид сапун се използва от хора с чувствителна, раздразнена и суха кожа.
Средствата с глицерин се използват при суха, лющеща се кожа, със сърбеж и кожни раздразнения.
Използването на глицерин вътре
Глицеринът е безопасен за хората и се използва като лекарство. Глицеринът се прилага вътре:
За отслабване;.
Подобряване на издръжливостта при упражнения, като помага на тялото да предотврати загубата на влага;
При диария и повръщане, за заместване на загубата на вода;
При глаукома за намаляване на очното налягане;
Интравенозният глицерин се прилага за намаляване на вътречерепното налягане при инсулт, менингит, енцефалит, синдром на Reine, травми и тумори на централната нервна система;
За намаляване на мозъчния оток по време на неврохирургични операции;
С припадък в нарушение на притока на кръв към мозъка.
Спортистите използват глицерин за предотвратяване на дехидратация.
Глицеринът се използва ректално като слабително средство. Действието на глицерина се основава на способността му да привлича вода в червата, като по този начин омекотява изпражненията и улеснява преминаването им през червата и предпазва от запек.
За възрастни нормата е 2-3 грама под формата на супозитории или 5-15 ml под формата на микроклистери.
За деца под шест години - 1-1,7 грама под формата на супозитории или 2-5 ml под формата на микроклистери.
Вредата на глицерина
Глицеринът е безопасен за повечето възрастни. Глицеринът не се отнася за средства, които предизвикват ферментация в организма и размножаване на бактерии. Резорбира се добре в тънките черва и не навлиза в дебелото черво.
Глицеринът няма вредни канцерогенни свойства, които увреждат ДНК и причиняват вродени ефекти. Основната вреда на глицерина за тялото е странични ефекти или дехидратация на тялото при неконтролирана употреба или без лекарско предписание.
Когато се приема през устата, глицеринът може да причини нежелани реакции, които могат да включват главоболие, замайване, подуване на корема, гадене, повръщане, жажда или диария. 
С повишено внимание глицеринът трябва да се използва за интравенозно приложение.
Няма данни за употребата на глицерин през устата при бременни и кърмещи жени. Ето защо е по-добре да откажете вътрешната употреба на глицерин в този момент.
Използването на глицерин като слабително може също да причини редица странични ефектикато сухота в устата, гадене, главоболие, диария, прекомерно уриниране, което в крайна сметка може да доведе до дехидратация.
Тъй като растителният глицерин се извлича главно от палмово или кокосово масло, той може да причини алергична реакция при хора, които са чувствителни към тези продукти.
Как се прилага глицерин
Нанесете глицерин в съответствие с инструкциите на опаковката. Ако не сте сигурни в точността на дадена информация, моля, консултирайте се с Вашия лекар.
Някои продукти, които съдържат глицерин, трябва да се разклатят преди употреба.
За да овлажните и омекотите кожата на ръцете, най-вероятно ще трябва да нанасяте глицерин всеки път, когато миете ръцете си.
Когато лекувате обрив от пелени, трябва да избършете кожата, където ще нанесете глицерин.
Когато използвате глицерин или продукт с него за лечение на кожни изгаряния след облъчване след лъчетерапия, трябва да проверите дали може да се използва след такава процедура.
Когато се прилага върху кожата, избягвайте контакт с очите, устата, носа.
ОПРЕДЕЛЕНИЕ
ГлицеролТова е безцветна, вискозна, сиропообразна течност, сладка на вкус. Не е отровен. Глицеринът е без мирис.
Неговите точки на топене и кипене са съответно 18 o C и 290 o C. Глицеринът е хигроскопичен, смесим с вода и етанол. Абсолютно чистият безводен глицерин се втвърдява при +18 o C, но е изключително трудно да се получи в твърда форма. Структурата на молекулата на глицерола е показана на фиг. един.
Ориз. 1. Структурата на молекулата на глицерина.
Глицеринът е широко разпространен в природата. Играе важна роля в метаболитните процеси в животинските организми, влиза в състава на повечето липиди - мазнини и други вещества, съдържащи се в животинските и растителните тъкани и изпълняващи най-важните функции в живите организми.
Получаване на глицерин
Най-старият метод за производство на глицерин е хидролизата на мазнини и масла:

Понастоящем глицеринът се получава синтетично от пропилей, който се образува по време на крекинг на масло. В този случай се използват различни начини за превръщане на пропилей в глицерол. Най-обещаващият метод е окисляването на пропилен с атмосферен кислород в присъствието на катализатор и при висока температура(kat = Cu, t 0 = 370). Процесът протича на няколко етапа.
Химични свойства на глицерина
Глицеринът е представител на тривалентните алкохоли, за които, както и за хидроксилсъдържащите съединения, са характерни същите реакции, както за едновалентните алкохоли.
Глицеринът реагира с активни метали (калий, натрий и др.), Които заместват водорода във всички хидроксилни групи, реагира с халогеноводороди (HCl, HBr и др.), В реакция на дехидратация, образувайки различни естери.
Глицеринът също има специфични свойства, които го отличават от едновалентните алкохоли: той реагира не само с алкални метали, но и с някои основи, включително неразтворими, например с меден (II) хидроксид:

Резултатът от реакцията на глицерол с меден (II) хидроксид е меден глицерат (сложно ярко синьо комплексно съединение). Тази реакция е качествена реакция към многовалентни алкохоли.
Най-важна в практическо отношение е реакцията на нитриране на глицерол, която води до образуването на тринитроглицерин C 3 H 5 (ONO 2) 3:

Приложение на глицерин
Глицеринът е съставка в много храни, кремове и козметика.
Примери за решаване на проблеми
ПРИМЕР 1
