Η γλυκερίνη αποκτά φυσικές και χημικές ιδιότητες. Φυσικές και χημικές ιδιότητες της γλυκερίνης και η εφαρμογή της. Πώς λαμβάνεται η γλυκερίνη;
Καλό απόγευμα φίλοι! Σήμερα θα μιλήσουμε για μια καταπληκτική ουσία - τη γλυκερίνη.
Η γλυκερίνη είναι μια αρκετά κοινή ουσία. Μπορεί να βρεθεί στη σύνθεση πολλών φαρμάκων, αλοιφών, κρεμών,σαπούνικαι μάλιστα μέσα σαμπουάν.
Πώς λαμβάνεται και πού χρησιμοποιείται;
Το κύριο μέρος της γλυκερίνης λαμβάνεται ως υποπροϊόν κατά τη σαπωνοποίηση των λιπών.
Το εύρος της γλυκερίνης είναι εκτεταμένο. Χρησιμοποιείται σε πολλές βιομηχανίες: βιομηχανίες ιατρικής, καπνού, κλωστοϋφαντουργίας, χαρτιού, χρωμάτων και βερνικιών, στην παραγωγή οικιακών χημικών, ηλεκτρονικών, ραδιομηχανικών κ.λπ.
Η γλυκερίνη, της οποίας οι ιδιότητες είναι τόσο διαφορετικές, χρησιμοποιείται ευρέως στο σπίτι. Για παράδειγμα, στη θεραπεία δερματικών παθήσεων και εγκαυμάτων, είναι αποτελεσματικό στον βήχα, έχει καθαρτική ιδιότητα και είναι το πιο απλό ενυδατικό.
Οι πιο συνηθισμένες συνταγές για τη χρήση γλυκερίνης στο σπίτι:
Glycerin Physico Χημικές ιδιότητεςαυτής της καταπληκτικής ουσίας, ας εξετάσουμε λεπτομερέστερα.
Χημικές ιδιότητες
Οι χημικές ιδιότητες της γλυκερίνης είναι ίδιες με αυτές των άλλων πολυϋδρικών αλκοολών. Και αυτό δεν είναι όλες οι ιδιότητες της γλυκερίνης. Ένα από τα πλεονεκτήματα της χρήσης γλυκερίνης είναι η χαμηλή τιμή και η διαθεσιμότητά της, επομένως οι μοναδικές της ιδιότητες μπορούν εύκολα να χρησιμοποιηθούν. Η γλυκερίνη μπορεί να αγοραστεί σε φαρμακεία ή ηλεκτρονικά καταστήματα.
Ας δούμε τις κύριες ιδιότητες της γλυκερίνης, οι οποίες θα είναι χρήσιμεςεφαρμογή .
Φυσικός ιδιότητες
 Η ιατρική γλυκερίνη είναι ένα άχρωμο παχύρρευστο υγρό, άοσμο, με γλυκιά γεύση. Γι' αυτό πήρε και το όνομά του («γλυκός» στα ελληνικά - γλυκό). Η γλυκερίνη είναι μη τοξική, διαλυτή στο νερό σε οποιαδήποτε ποσότητα, είναι καλός διαλύτης για ανόργανα άλατα, αλκάλια, μονο- και δισακχαρίτες.
Η ιατρική γλυκερίνη είναι ένα άχρωμο παχύρρευστο υγρό, άοσμο, με γλυκιά γεύση. Γι' αυτό πήρε και το όνομά του («γλυκός» στα ελληνικά - γλυκό). Η γλυκερίνη είναι μη τοξική, διαλυτή στο νερό σε οποιαδήποτε ποσότητα, είναι καλός διαλύτης για ανόργανα άλατα, αλκάλια, μονο- και δισακχαρίτες.
Υγροσκοπικότητα- την ικανότητα των ουσιών να απορροφούν την υγρασία από τον αέρα
Γλυκερίνη σε καθαρή μορφήυγροσκοπικό, δηλαδή είναι σε θέση να απομακρύνει την υγρασία (απορροφά νερό έως και το 40% του βάρους του), άρα μπορεί να στεγνώσει το δέρμα. Όμως στην ποσότητα (ποσοστό συνήθως δεν ξεπερνά το 7%), στην οποία χρησιμοποιείται στην κοσμετολογία, έχει το αντίθετο (ενυδατικό) αποτέλεσμα. Η γλυκερίνη έχει βρει ευρεία εφαρμογή ως ενυδατικό και μαλακτικό.
Αφού χρησιμοποιήσετε ένα καλλυντικό προϊόν με προσθήκη γλυκερίνης, το δέρμα σας θα είναι ενυδατωμένο, απαλό, λείο και ελαστικό. Στην καθαρή του μορφή, αντίθετα, θα στεγνώσει το δέρμα, επομένως δεν χρησιμοποιείται ξεχωριστά στην κοσμετολογία.

Η γλυκερίνη αντλεί υγρασία από τον περιβάλλοντα αέρα και διαποτίζει το δέρμα μας με αυτήν, σχηματίζοντας ένα υγρό φιλμ στην επιφάνεια του δέρματος. Τι γίνεται αν ο αέρας είναι ξηρός; Σε αυτή την περίπτωση, η γλυκερίνη θα πάρει την υγρασία από τα στρώματα του δέρματος, στεγνώνοντάς το.
Αυτός είναι ο λόγος για τον οποίο είναι απαραίτητο να τηρείτε ορισμένους κανόνες όταν χρησιμοποιείτε γλυκερίνη στα καλλυντικά.:
Μην χρησιμοποιείτε καθαρή γλυκερίνη και μην χρησιμοποιείτε προϊόντα με γλυκερίνη σε ξηρά κλίματα.
Διαλυτότητα
Η γλυκερίνη είναι ικανή να διαλύει διάφορα οργανικά και μη οργανική ύλη: ιώδιο, αλκάλια, διάφορα άλατα, σάκχαρα κ.λπ. Ενισχύει την καθαριστική δύναμη των προϊόντων καθαρισμού. Είναι συχνός επισκέπτης στη σύνθεση των καθαριστικών γυαλιού, θα βοηθήσει στην απομάκρυνση των λιπαρών λεκέδων.
Πλαστική ύλη
Η γλυκερίνη ενισχύει το απορρυπαντικό συστατικόσαπούνι και του προσδίδει πλαστικότητα. Χάρη σε αυτό, δουλεύοντας με σαπούνι βάση με γλυκερίνηευκολότερη και περισσότερες ευκαιρίες για την υλοποίηση ιδεών. Η ίδια ιδιότητα της γλυκερίνης χρησιμοποιείται για την κάλυψη της χαμηλής ποιότητας. Η κακή βότκα, εάν προστεθεί γλυκερίνη σε αυτήν, δεν παγώνει στο κρύο, αλλά γίνεται λίγο παχύρρευστη, σαν ένα ανάλογο υψηλής ποιότητας. Επομένως, εάν συναντάτε γλυκερίνη στη σύνθεση της βότκας, βγάλτε τα κατάλληλα συμπεράσματα.

αντισηπτικό
Η γλυκερίνη είναι ένα εξαιρετικό αντισηπτικό. Πιθανότατα έχετε παρατηρήσει ότι όταν εφαρμόζετε μια κρέμα με προσθήκη γλυκερίνης, οι πληγές επουλώνονται πιο γρήγορα.
Συχνά ένας συνδυασμός πολλών ιδιοτήτων γλυκερίνης χρησιμοποιείται ταυτόχρονα. Για παράδειγμα, η γλυκερίνη χρησιμοποιείται ως μαλακτικό στην κατασκευή υφασμάτων και δέρματος λόγω της πλαστικότητας και της υγροσκοπικότητας της. Στο σπίτι μπορεί να βοηθήσει στην επαναφορά.
Για καλλυντικούς σκοπούς Η γλυκερίνη είναι σημαντική για την κατασκευή μαλακτικών, ενυδατικών και καθαριστικών μασκών, λοσιόν, κρεμών. Όπως κάθε φυσικό προϊόν, είναι καλύτερα αποδεκτό από το δέρμα παρά ένα συνθετικό προϊόν.
Μάσκες γλυκερίνης χρήσιμο όχι  μόνο όταν φροντίζετε το δέρμα του προσώπου και των χεριών, αλλά θα χρησιμεύσει και ως εξαιρετική υπηρεσία όταν
μόνο όταν φροντίζετε το δέρμα του προσώπου και των χεριών, αλλά θα χρησιμεύσει και ως εξαιρετική υπηρεσία όταν
Πολυϋδρικές αλκοόλες- Πρόκειται για οργανικές ενώσεις των οποίων τα μόρια περιέχουν δύο ή περισσότερες υδροξυλομάδες συνδεδεμένες με μια ρίζα υδρογονάνθρακα.
Οι ομάδες ΟΗ στις πολυϋδρικές αλκοόλες βρίσκονται σε διαφορετικά άτομα άνθρακα:
Οι ενώσεις με δύο ομάδες ΟΗ σε ένα άτομο άνθρακα είναι ασταθείς. Διασπούν το νερό και μετατρέπονται σε αλδεΰδες:
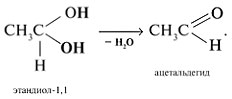
Οι ενώσεις με δύο ομάδες ΟΗ σε γειτονικά άτομα άνθρακα ονομάζονται γλυκόλες (ή διόλες).
Παραλαβή
Οι γλυκόλες λαμβάνονται με την οξείδωση των αλκενίων σε ένα υδατικό μέσο. Για παράδειγμα, υπό τη δράση του υπερμαγγανικού καλίου ή του ατμοσφαιρικού οξυγόνου παρουσία ενός καταλύτη αργύρου, τα αλκένια μετατρέπονται σε διυδρικές αλκοόλες:

Ένας άλλος τρόπος για τη λήψη πολυυδρικών αλκοολών είναι η υδρόλυση των παραγώγων αλογόνου των υδρογονανθράκων:
Κατά την παραγωγή, η γλυκερίνη λαμβάνεται σύμφωνα με το σχήμα:

Φυσικές ιδιότητες
Η αιθυλενογλυκόλη και η γλυκερίνη είναι άχρωμα παχύρρευστα υγρά με γλυκιά γεύση (από τα ελληνικά - γλυκιά). Η διαλυτότητα στο νερό είναι απεριόριστη. Σημεία βρασμού αιθυλενογλυκόλης - 197,2 °C, γλυκερίνης - 290 °C. Η αιθυλενογλυκόλη είναι δηλητήριο.
Χημικές ιδιότητες
Η αιθυλενογλυκόλη και η γλυκερίνη είναι παρόμοια με τις μονοϋδρικές αλκοόλες.
Έτσι αντιδρούν με ενεργά μέταλλα:

Πολυϋδρικές αλκοόλες σε αντίδραση με υδραλογονίδιαανταλλάσσουν μία ή περισσότερες ομάδες υδροξυλίου ΟΗ με άτομα αλογόνου:

Η γλυκερίνη αλληλεπιδρά με νιτρικό οξύγια σχηματισμό εστέρων. Ανάλογα με τις συνθήκες αντίδρασης (μοριακή αναλογία αντιδραστηρίων, συγκέντρωση καταλύτη - θειικό οξύ και θερμοκρασία), λαμβάνονται μονο-, δι- και τρινιτρογλυκερίδια:

Ποιοτική αντίδραση πολυϋδρικών αλκοολών, που καθιστά δυνατή τη διάκριση ενώσεων αυτής της κατηγορίας, είναι η αλληλεπίδραση με πρόσφατα παρασκευασμένο υδροξείδιο του χαλκού (II). Σε ένα αλκαλικό περιβάλλον με επαρκή συγκέντρωση γλυκερόλης, το μπλε ίζημα Cu (OH) 2 διαλύεται για να σχηματίσει ένα φωτεινό μπλε διάλυμα - γλυκολικό χαλκό (II):

 |
ΓΥΜΝΑΣΙΑ.
1. Υπογραμμίστε τους συντακτικούς τύπους των πολυϋδρικών αλκοολών:
СlCH 2 CH 2 Cl, HOS 3 H 7, NOCH 2 CH 2 OH, C 2 H 6 O 2, 
NOCH 2 COOH, NOCH 2 CH 2 CH 2 OH, CH 3 OCH 2 CH 2 OH.
2. Να συνθέσετε τους συντακτικούς τύπους τους με τα ονόματα των ουσιών:
α) αιθανοδιόλη-1,2; β) αιθυλενογλυκόλη. γ) προπανοδιόλη-1,2· δ) προπανοδιόλη-1,3·
ε) γλυκερίνη; στ) βουτανοτριόλη-1,2,4.
3.
Γράψτε τις εξισώσεις αντίδρασης για την παραγωγή αιθυλενογλυκόλης από:
α) αιθυλένιο. β) 1,2-διβρωμοαιθάνιο.
4. Να αναφέρετε πέντε τομείς εφαρμογής πολυυδρικών αλκοολών (αιθυλενογλυκόλη και γλυκερίνη).
5. Να γράψετε εξισώσεις αντίδρασης για μια αλυσίδα χημικών μετασχηματισμών, να ονομάσετε οργανικές ουσίες:
6.
Κάντε μια αλυσίδα χημικών μετασχηματισμών για να λάβετε διυδρική αλκοόλη
CH 3 CHONCH 2 OH από αλκάνιο C 3 H 8 . Χρησιμοποιήστε το σχήμα:
κορεσμένος υδρογονάνθρακας μονοαλογονοϋδρογονάνθρακας ακόρεστος υδρογονάνθρακας διαλοϋδρογονάνθρακας διυδρική αλκοόλη.
Απαντήσεις στις ασκήσεις για το θέμα 2
Μάθημα 20
1. Οι δομικοί τύποι των πολυϋδρικών αλκοολών υπογραμμίζονται:
2. Δομικοί τύποι που συντάσσονται με τα ονόματα των ουσιών:
3. Αντιδράσεις για τη λήψη αιθυλενογλυκόλης:

4. Πέντε τομείς εφαρμογής πολυυδρικών αλκοολών.
αιθυλενογλυκόλη(EG) - σε αντιψυκτικό, το 66% EG παγώνει στους -60 ° C.
στη σύνθεση του lavsan [–CH 2 CH 2 O(O) CC(O)O–] n;
διαλύτης ( t bp = 198 °C).
Γλυκερίνη- στην αρωματοποιία, τα καλλυντικά, την ιατρική - ένας διαλύτης, ένα συστατικό αλοιφών.
για την παραγωγή τρινιτρογλυκερίνης - ένα εκρηκτικό και ένα φάρμακο που διαστέλλει τα αιμοφόρα αγγεία.
5. Αντιδράσεις για μια αλυσίδα χημικών μετασχηματισμών:

6. Η αλυσίδα των χημικών μετασχηματισμών του C 3 H 8 αλκανίου σε προπυλενογλυκόλη CH 3 CHOHCH 2 OH μέσω ενδιάμεσων ουσιών δεδομένων κατηγοριών.
Η γλυκερίνη ή, σύμφωνα με τη διεθνή ονοματολογία, η προπανετριόλη -1,2,3, είναι μια σύνθετη ουσία που ανήκει στις πολυϋδρικές αλκοόλες, ή μάλλον, είναι μια τριυδρική αλκοόλη, γιατί. έχει 3 υδροξυλομάδες - ΟΗ. Οι χημικές ιδιότητες της γλυκερίνης είναι παρόμοιες με αυτές της γλυκερίνης, αλλά είναι πιο έντονες λόγω του ότι υπάρχουν περισσότερες υδροξυλομάδες και επηρεάζουν η μία την άλλη.
Η γλυκερίνη, όπως και οι αλκοόλες με μία ομάδα υδροξυλίου, είναι εξαιρετικά διαλυτή στο νερό. Αυτό, θα έλεγε κανείς, είναι επίσης μια ποιοτική αντίδραση στη γλυκερίνη, αφού διαλύεται στο νερό σχεδόν σε οποιαδήποτε αναλογία. Αυτή η ιδιότητα χρησιμοποιείται στην παραγωγή αντιψυκτικών - υγρών που δεν παγώνουν και ψύχουν τους κινητήρες των αυτοκινήτων και των αεροσκαφών.
Η γλυκερίνη αλληλεπιδρά επίσης με το υπερμαγγανικό κάλιο. Αυτή είναι μια ποιοτική αντίδραση στη γλυκερίνη, η οποία ονομάζεται επίσης ηφαίστειο Scheele. Για να το εκτελέσετε, είναι απαραίτητο να προσθέσετε 1-2 σταγόνες άνυδρης γλυκερίνης στη σκόνη υπερμαγγανικού καλίου, η οποία χύνεται με τη μορφή διαφάνειας με εσοχή σε ένα πορσελάνινο μπολ. Μετά από ένα λεπτό, το μείγμα αναφλέγεται αυθόρμητα.Κατά τη διάρκεια της αντίδρασης, απελευθερώνεται μεγάλη ποσότητα θερμότητας και θερμά σωματίδια προϊόντων αντίδρασης και υδρατμοί διασπώνται. Αυτή η αντίδραση είναι οξειδοαναγωγή.

Η γλυκερίνη είναι υγροσκοπική, δηλ. ικανό να συγκρατήσει την υγρασία. Σε αυτή την ιδιότητα βασίζεται η ακόλουθη ποιοτική αντίδραση στη γλυκερίνη. Πραγματοποιείται σε απαγωγέα καπνού. Για να το εκτελέσετε, ρίξτε περίπου 1 cm3 κρυσταλλικού όξινου θειικού καλίου (KHSO4) σε έναν καθαρό, στεγνό δοκιμαστικό σωλήνα. Προσθέστε 1-2 σταγόνες γλυκερίνη και στη συνέχεια ζεστάνετε μέχρι να εμφανιστεί μια έντονη μυρωδιά. Το όξινο θειικό κάλιο δρα εδώ ως μια ουσία που απορροφά το νερό, η οποία αρχίζει να εκδηλώνεται όταν θερμαίνεται. Η γλυκερίνη, χάνοντας νερό, μετατρέπεται σε μια ακόρεστη ένωση - ακρολεΐνη, η οποία έχει μια έντονη δυσάρεστη οσμή. C3H5(OH)3 - H2C=CH-CHO + 2 H2O.
Η αντίδραση της γλυκερίνης με το υδροξείδιο του χαλκού είναι ποιοτική και χρησιμεύει για τον προσδιορισμό όχι μόνο της γλυκερίνης, αλλά και άλλων.Για να πραγματοποιηθεί, είναι αρχικά απαραίτητο να παρασκευαστεί ένα φρέσκο διάλυμα υδροξειδίου του χαλκού (II). Για να γίνει αυτό, προσθέτουμε και παίρνουμε υδροξείδιο του χαλκού (II), το οποίο σχηματίζει ένα μπλε ίζημα. Προσθέτουμε μερικές σταγόνες γλυκερίνης σε αυτόν τον δοκιμαστικό σωλήνα με ένα ίζημα και παρατηρούμε ότι το ίζημα έχει εξαφανιστεί και το διάλυμα έχει αποκτήσει μπλε χρώμα.

Το σύμπλοκο που προκύπτει ονομάζεται αλκοολικός ή γλυκερικός χαλκός. Η ποιοτική αντίδραση για τη γλυκερίνη με υδροξείδιο του χαλκού (II) χρησιμοποιείται εάν η γλυκερίνη είναι σε καθαρή μορφή ή σε υδατικό διάλυμα. Για να πραγματοποιηθούν τέτοιες αντιδράσεις στις οποίες η γλυκερίνη είναι με ακαθαρσίες, είναι απαραίτητο να προκαθαριστεί από αυτές.
Οι ποιοτικές αντιδράσεις στη γλυκερίνη βοηθούν στον εντοπισμό της σε οποιοδήποτε περιβάλλον. Αυτό χρησιμοποιείται ενεργά για τον προσδιορισμό της γλυκερίνης σε τρόφιμα, καλλυντικά, αρώματα, φάρμακα και αντιψυκτικά.
Η γλυκερίνη είναι ένα παχύρρευστο, άχρωμο υγρό με ελαφρώς γλυκιά γεύση. Η γλυκερίνη είναι ασφαλής για ανθρώπινη κατανάλωση. Βρίσκεται σε πολλά προϊόντα, από καραμέλα μέχρι οδοντόκρεμα. Η ευρεία χρήση της γλυκερίνης στη φαρμακευτική, ζαχαροπλαστική, καλλυντική και άλλες βιομηχανίες οφείλεται στις ιδιότητές της.
Ιδιότητες της γλυκερίνης
Η γλυκερίνη είναι οργανική ένωση. Η γλυκερίνη λαμβάνεται από φυτικά και ζωικά έλαια. Η γλυκερίνη είναι πολύ διαλυτή στο νερό και το αλκοόλ. Από την άλλη πλευρά, πολλές ουσίες που είναι ελάχιστα διαλυτές σε αλκοόλ και νερό μπορούν να διαλυθούν στη γλυκερίνη. Από αυτό μπορούμε να συμπεράνουμε ότι η γλυκερίνη είναι ένας καλός διαλύτης.
Η γλυκερίνη είναι 1500 φορές πιο παχύρρευστη από το νερό. Αυτό το παχύρρευστο διαφανές υγρό έχει υψηλό σημείο βρασμού και πρακτικά δεν παγώνει.
Δεδομένου ότι η γλυκερίνη δεν αντιδρά με έλαια και επομένως είναι πιο ανθεκτική στην οξείδωση από τις ορυκτές ουσίες, η γλυκερίνη μπορεί να χρησιμοποιηθεί ως λιπαντικό. Μπορεί να χρησιμοποιηθεί για τη λίπανση εξαρτημάτων και μηχανικών μερών που εκτίθενται σε βενζόλιο ή βενζίνη, καθώς δεν διαλύονται στη γλυκερίνη.
Το διαφανές χρώμα του επιτρέπει τη χρήση του σε πολλές βιομηχανίες, καθώς δεν επηρεάζει σε καμία περίπτωση το χρώμα του τελικού προϊόντος.
Η γλυκερίνη είναι υγροσκοπικό υγρό. Εάν ρίξετε καθαρή γλυκερίνη στη γλώσσα σας, μπορεί να καείτε. Αλλά όταν αραιώνεται με νερό, η γλυκερίνη ενυδατώνει καλά το δέρμα.
Πώς λαμβάνεται η γλυκερίνη;
Η γλυκερίνη είναι ένα υποπροϊόν στη σαπωνοποιία. Μέχρι το 1889, δεν ήξεραν πώς να αποκαταστήσουν στη διαδικασία της σαπουνοποιίας.
Το 1889 βρέθηκε ένας τρόπος διαχωρισμού της γλυκερίνης από το σαπούνι. Η κύρια χρήση του εκείνη την εποχή ήταν η παραγωγή νιτρογλυκερίνης, από την οποία παρασκευαζόταν δυναμίτης.
Η διαδικασία αφαίρεσης της γλυκερίνης από το σαπούνι είναι αρκετά περίπλοκη. Το σαπούνι παρασκευάζεται από φυτικά ή ζωικά λίπη, τα οποία περιέχουν ήδη γλυκερίνη στη σύνθεσή του από 7 έως 13 τοις εκατό. Όταν τα λίπη αντιδρούν με αλκάλια, λαμβάνεται σαπούνι. Αλλά η γλυκερίνη βρίσκεται στο ίδιο το σαπούνι.
Όταν προστίθεται αλάτι, το σαπούνι διαχωρίζεται και η γλυκερίνη και άλλες ακαθαρσίες υπάρχουν στο υπόλοιπο υγρό υπόλειμμα. Η γλυκερίνη στη συνέχεια διαχωρίζεται με υδρόλυση και περαιτέρω καθαρίζεται με διήθηση μέσω φίλτρων άνθρακα ή με άλλες μεθόδους. 
Σύνθεση γλυκερίνης
Η γλυκερίνη έχει μοριακός τύπος C3H5 (OH) 3. Αποτελείται από μια αλυσίδα τριών ατόμων άνθρακα, έτσι ώστε κάθε άτομο άνθρακα να συνδέεται με ένα άτομο υδρογόνου (Η+) και μια ομάδα υδροξυλίου (ΟΗ-). Καθένας από τους δύο τερματικούς άνθρακες έχει ένα επιπλέον άτομο υδρογόνου, έτσι ώστε και οι τρεις άνθρακες να έχουν συνολικά τέσσερις δεσμούς. Ο άνθρακας έχει σθένος τεσσάρων, που σημαίνει ότι τείνει να σχηματίζει τέσσερις δεσμούς.
Τα λιπαρά οξέα είναι μια κατηγορία ενώσεων που είναι ουσιαστικά μια μακρά αλυσίδα ατόμων άνθρακα που συνδέονται με διάφορους συνδυασμούς ατόμων οξυγόνου και υδρογόνου. Κάθε μόριο λιπαρού οξέος τελειώνει με ένα άτομο άνθρακα που σχηματίζει έναν διπλό δεσμό με ένα άτομο οξυγόνου και έναν απλό δεσμό με μια ομάδα υδροξυλίου. Αυτή η ομάδα έχει τον τύπο COOH- και ονομάζεται καρβοξυλική ομάδα.
Τα τριγλυκερίδια είναι εστέρες γλυκερόλης με μακράς αλυσίδας καρβοξυλικά οξέα.
Εφαρμογή γλυκερίνης
Η γλυκερίνη χρησιμοποιείται σε πολλούς τομείς, συμπεριλαμβανομένης της ιατρικής.
βιομηχανία τροφίμων
Στα τρόφιμα και τα ποτά, η γλυκερίνη χρησιμεύει ως υγραντικό, διαλύτης και γλυκαντικό. Χρησιμοποιείται για την παραγωγή προϊόντων με λίγες θερμίδες ως υποκατάστατο του λίπους, ως πυκνωτικό στα λικέρ.
Η γλυκερίνη χρησιμοποιείται επίσης ως υποκατάστατο ζάχαρης. Σε αντίθεση με τη ζάχαρη, αναστέλλει την ανάπτυξη βακτηρίων. Επιπλέον, η γλυκερίνη έχει χαμηλότερο γλυκαιμικό δείκτη. Στα προϊόντα διατροφής, η γλυκερίνη χαρακτηρίζεται ως E 422.
Η γλυκερίνη στην ιατρική
Στην ιατρική, η γλυκερίνη χρησιμοποιείται σε σιρόπια για τον βήχα, ελιξίρια και αποχρεμπτικά. Χρησιμοποιείται στην κατασκευή οδοντόκρεμων, στοματικών πλύσεων.
Σε στερεά φάρμακα όπως τα δισκία, η γλυκερίνη χρησιμοποιείται ως παράγοντας συγκράτησης νερού.
Η γλυκερίνη έχει καθαρτικές ιδιότητες και χρησιμοποιείται ως καθαρτικό σε υπόθετα ή με τη μορφή μικροκλυστέρων.
Η γλυκερίνη που αναμιγνύεται συχνότερα με χυμό φρούτων για τη μείωση της γλυκιάς γεύσης μπορεί να ληφθεί ως η πρώτη θεραπεία έκτακτης ανάγκης για αυξημένη πίεση στα μάτια. Μειώνει γρήγορα την ενδοφθάλμια πίεση.
Η γλυκερίνη έχει διουρητική δράση, που σημαίνει ότι μπορεί να συμβάλει στην αφυδάτωση και δεν πρέπει να χρησιμοποιείται τακτικά. 
Γλυκερίνη στα καλλυντικά
Στα καλλυντικά, η γλυκερίνη χρησιμοποιείται ως ενυδατικό συστατικό σε προϊόντα περιποίησης δέρματος, κρέμες ξυρίσματος και άλλα προϊόντα προσωπικής φροντίδας.
Η γλυκερίνη είναι το κύριο συστατικό του σαπουνιού γλυκερίνης. Αυτό το είδος σαπουνιού χρησιμοποιείται από άτομα με ευαίσθητο, ερεθισμένο και ξηρό δέρμα.
Τα μέσα με γλυκερίνη χρησιμοποιούνται για ξηρό, ξεφλουδισμένο δέρμα, με δερματικό κνησμό και δερματικούς ερεθισμούς.
Η χρήση γλυκερίνης στο εσωτερικό
Η γλυκερίνη είναι ασφαλής για τον άνθρωπο και χρησιμοποιείται ως φάρμακο. Η γλυκερίνη εφαρμόζεται στο εσωτερικό:
Για απώλεια βάρους?
Βελτίωση της αντοχής στην άσκηση βοηθώντας το σώμα να αποτρέψει την απώλεια υγρασίας.
Κατά τη διάρκεια της διάρροιας και του εμέτου, για την αντικατάσταση της απώλειας νερού.
Με γλαύκωμα για μείωση της πίεσης των ματιών.
Η ενδοφλέβια γλυκερίνη χορηγείται για τη μείωση της ενδοκρανιακής πίεσης σε εγκεφαλικό επεισόδιο, μηνιγγίτιδα, εγκεφαλίτιδα, σύνδρομο Reine, τραύμα και όγκους του κεντρικού νευρικού συστήματος.
Για τη μείωση του εγκεφαλικού οιδήματος κατά τη διάρκεια νευροχειρουργικών επεμβάσεων.
Με λιποθυμία σε παραβίαση της ροής του αίματος στον εγκέφαλο.
Οι αθλητές χρησιμοποιούν γλυκερίνη για να αποτρέψουν την αφυδάτωση.
Η γλυκερίνη χρησιμοποιείται από το ορθό ως καθαρτικό. Η δράση της γλυκερίνης βασίζεται στην ικανότητά της να προσελκύει νερό στα έντερα, μαλακώνοντας έτσι τα κόπρανα και διευκολύνοντας τη διέλευσή τους κατά μήκος των εντέρων και αποτρέποντας τη δυσκοιλιότητα.
Για τους ενήλικες, ο κανόνας είναι 2-3 γραμμάρια με τη μορφή υπόθετου ή 5-15 ml με τη μορφή μικροκλυστέρων.
Για παιδιά ηλικίας κάτω των έξι ετών - 1-1,7 γραμμάρια με τη μορφή υπόθετων ή 2-5 ml με τη μορφή μικροκλυστέρων.
Η βλάβη της γλυκερίνης
Η γλυκερίνη είναι ασφαλής για τους περισσότερους ενήλικες. Η γλυκερίνη δεν εφαρμόζεται στα μέσα που προκαλούν ζύμωση στο σώμα και την αναπαραγωγή βακτηρίων. Απορροφάται καλά στο λεπτό έντερο και δεν εισέρχεται στο παχύ έντερο.
Η γλυκερίνη δεν έχει επιβλαβείς καρκινογόνες ιδιότητες που βλάπτουν το DNA και προκαλούν έμφυτες επιδράσεις. Η κύρια βλάβη της γλυκερίνης για τον οργανισμό είναι οι παρενέργειες ή η αφυδάτωση του οργανισμού με ανεξέλεγκτη χρήση ή χωρίς συνταγή γιατρού.
Όταν λαμβάνεται από το στόμα, η γλυκερίνη μπορεί να προκαλέσει παρενέργειες που μπορεί να περιλαμβάνουν πονοκεφάλους, ζάλη, φούσκωμα, ναυτία, έμετο, δίψα ή διάρροια. 
Με προσοχή, η γλυκερίνη πρέπει να χρησιμοποιείται για ενδοφλέβια χρήση.
Δεν υπάρχουν δεδομένα για τη χρήση της γλυκερίνης από το στόμα σε έγκυες και θηλάζουσες γυναίκες. Επομένως, είναι καλύτερο να αρνηθείτε την εσωτερική χρήση γλυκερίνης αυτή τη στιγμή.
Η χρήση της γλυκερίνης ως καθαρτικό μπορεί επίσης να προκαλέσει μια σειρά από παρενέργειεςόπως ξηροστομία, ναυτία, πονοκέφαλο, διάρροια, υπερβολική ούρηση, που μπορεί τελικά να οδηγήσει σε αφυδάτωση.
Δεδομένου ότι η φυτική γλυκερίνη προέρχεται κυρίως από φοινικέλαιο ή λάδι καρύδας, μπορεί να προκαλέσει αλλεργική αντίδραση σε άτομα που είναι ευαίσθητα σε αυτά τα προϊόντα.
Πώς να εφαρμόσετε γλυκερίνη
Εφαρμόστε γλυκερίνη σύμφωνα με τις οδηγίες στη συσκευασία. Εάν δεν είστε σίγουροι για την ακρίβεια οποιασδήποτε πληροφορίας, συμβουλευτείτε το γιατρό σας.
Ορισμένα προϊόντα που περιέχουν γλυκερίνη πρέπει να ανακινηθούν πριν από τη χρήση.
Για να ενυδατώσετε και να μαλακώσετε το δέρμα των χεριών, πιθανότατα θα χρειαστεί να βάζετε γλυκερίνη κάθε φορά που πλένετε τα χέρια σας.
Όταν αντιμετωπίζετε το εξάνθημα από την πάνα, πρέπει να σκουπίσετε το δέρμα όπου θα εφαρμόσετε γλυκερίνη.
Όταν χρησιμοποιείτε γλυκερίνη ή ένα προϊόν μαζί της για τη θεραπεία δερματικών εγκαυμάτων μετά από ακτινοβολία μετά από ακτινοθεραπεία, πρέπει να ελέγξετε εάν μπορεί να χρησιμοποιηθεί μετά από μια τέτοια διαδικασία.
Όταν εφαρμόζεται στο δέρμα, αποφύγετε την επαφή με τα μάτια, το στόμα, τη μύτη.
ΟΡΙΣΜΟΣ
ΓλυκερίνηΕίναι ένα άχρωμο, παχύρρευστο, σιροπιαστό υγρό, με γλυκιά γεύση. Όχι δηλητηριώδες. Η γλυκερίνη είναι άοσμη.
Τα σημεία τήξης και βρασμού του είναι 18 o C και 290 o C, αντίστοιχα. Η γλυκερίνη είναι υγροσκοπική, αναμίξιμη με νερό και αιθανόλη. Η απολύτως καθαρή άνυδρη γλυκερίνη στερεοποιείται στους +18 o C, αλλά είναι εξαιρετικά δύσκολο να ληφθεί σε στερεή μορφή. Η δομή του μορίου της γλυκερίνης φαίνεται στο σχ. ένας.
Ρύζι. 1. Η δομή του μορίου της γλυκερίνης.
Η γλυκερίνη είναι ευρέως διαδεδομένη στη φύση. Παίζει σημαντικό ρόλο στις μεταβολικές διεργασίες στους ζωικούς οργανισμούς· είναι μέρος των περισσότερων λιπιδίων - λιπών και άλλων ουσιών που περιέχονται στους ζωικούς και φυτικούς ιστούς και εκτελεί τις πιο σημαντικές λειτουργίες στους ζωντανούς οργανισμούς.
Λήψη γλυκερίνης
Η παλαιότερη μέθοδος για την παραγωγή γλυκερίνης είναι η υδρόλυση λιπών και ελαίων:

Επί του παρόντος, η γλυκερίνη λαμβάνεται συνθετικά από προπυλένιο, το οποίο σχηματίζεται κατά τη διάσπαση του λαδιού. Σε αυτή την περίπτωση, χρησιμοποιούνται διαφορετικοί τρόποι μετατροπής του προπυλενίου σε γλυκερίνη. Η πιο πολλά υποσχόμενη μέθοδος είναι η οξείδωση του προπυλενίου με ατμοσφαιρικό οξυγόνο παρουσία καταλύτη και σε υψηλή θερμοκρασία(kat = Cu, t 0 = 370). Η διαδικασία προχωρά σε διάφορα στάδια.
Χημικές ιδιότητες της γλυκερίνης
Η γλυκερίνη είναι αντιπροσωπευτική των τριυδρικών αλκοολών, για τις οποίες, όπως και για τις ενώσεις που περιέχουν υδροξύλιο, οι ίδιες αντιδράσεις είναι χαρακτηριστικές με τις μονοϋδρικές αλκοόλες.
Η γλυκερίνη αντιδρά με ενεργά μέταλλα (κάλιο, νάτριο κ.λπ.) που αντικαθιστούν το υδρογόνο σε όλες τις υδροξυλομάδες, αντιδρά με υδραλογονίδια (HCl, HBr κ.λπ.), σε αντίδραση αφυδάτωσης, σχηματίζοντας διάφορους εστέρες.
Η γλυκερίνη έχει επίσης συγκεκριμένες ιδιότητες που τη διακρίνουν από τις μονοϋδρικές αλκοόλες: αντιδρά όχι μόνο με αλκαλικά μέταλλα, αλλά και με ορισμένες βάσεις, συμπεριλαμβανομένων των αδιάλυτων, για παράδειγμα, με υδροξείδιο του χαλκού (II):

Το αποτέλεσμα της αντίδρασης της γλυκερόλης με το υδροξείδιο του χαλκού (II) είναι ο γλυκερικός χαλκός (μια σύνθετη σύνθετη ένωση φωτεινού μπλε). Αυτή η αντίδραση είναι μια ποιοτική αντίδραση σε πολυϋδρικές αλκοόλες.
Η πιο σημαντική από πρακτική άποψη είναι η αντίδραση νίτρωσης της γλυκερίνης, η οποία οδηγεί στο σχηματισμό της τρινιτρογλυκερίνης C 3 H 5 (ONO 2) 3:

Εφαρμογή γλυκερίνης
Η γλυκερίνη είναι συστατικό σε πολλά τρόφιμα, κρέμες και καλλυντικά.
Παραδείγματα επίλυσης προβλημάτων
ΠΑΡΑΔΕΙΓΜΑ 1
