Резорцин реакции. Химический опыт – получаем флуоресцеин. Получение из галогенбензолов
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Синтез флуоресцеина
Решил провести эксперименты с флуоресцеином, но готового реактива под рукой не оказалось: пришлось провести пробный синтез. В наличии были фталевый ангидрид и несколько грамм резорцина. За основу взял методику из статьи .
Для пробного эксперимента необходимые количества веществ рассчитывать не стал: просто взял 1 гр фталевого ангидрида, 1 гр резорцина, смешал. Смесь поместил в стаканчик на 50 мл и смочил примерно 0.5 мл концентрированной серной кислоты.
Стаканчик закрепил над включенной электрической плиткой. Смесь расплавилась и стала малиновой. Позже - красновато-коричневой. Нагрев регулировал, то убирая, то подставляя под стаканчик плитку. В целом смесь несильно кипела минут 5. Когда стаканчик снял с плитки, в верхней его части образовались иглы фталевого ангидрида.
Приготовил раствор 0.5 гр едкого натра в 50 мл воды. Смесь нужно было вылить из стаканчика в раствор щелочи, не дав ей остыть - иначе она застынет. В случае с пробиркой (см. цитируемую статью) это, видимо, было несложно, но у стаканчика бОльшая поверхность - смесь застывала. Из стаканчика удалось вылить в раствор щелочи всего лишь несколько капель, которые застыли на дне в виде зеленых шариков. Раствор стал желтовато-зеленым с характерной флуоресценцией.
Остальную часть застывшего расплава было достать из стакана проблематично. Решил: "Если гора не идет к Магомету - не грех сходить к горе". Вместо того чтобы пытаться выколупывать продукт, чтобы перенести его в щелочь, лучше налить щелочь в стакан с застывшей реакционной смесью и подождать, пока она растворится.
В результате получилась темно-зеленая жидкость с осадком. Поставил стаканчик на выключенную, но все еще горячую плитку. Реакционная смесь постепенно отстала от стенок, а жидкость стала коричневой.
Так и оставил на выходные. Потом еще переживал, что стакан нужно было накрыть, чтобы флуоресцеин в щелочной среде не окислялся воздухом (указаний на такую опасность в литературе не встречал, но кто его знает...)
После выходных пришел на работу и посмотрел на свой флуоресцеин (в пятницу оставил стакан с плавом, залитым раствором щелочи на остывающей плитке).
В стакане был желтый раствор (натриевая соль флуоресцеина - уранин) и красный порошок - осадок флуоресцеина. Однако не весь осадок был в виде порошка. На стеклянную палочку налипла масса, похожая на карамель (нерастворившийся плав).
Содержимое стакана профильтровал: образовался желтый раствор, а красный осадок осел на фильтре.
Когда я посмотрел методику получения флуоресцеина из резорцина и фталевого ангидрида , то убедился, что взял фталевый ангидрид в избытке (на 22.5 г резорцина нужно 15 г фталевого ангидрида, я же взял наугад: 1 г резорцина - 1 г фталевого ангидрида).
Именно поэтому не весь плав растворился, среда в стакане была явно не щелочной, а большая часть флуоресцеина находилась в осадке (напомню: флуоресцеин слабо растворим в воде, а его натриевая соль [уранин] - значительно лучше).
Палочку с прилипшей к ней массой перенес в чистый стакан, добавил гранулы едкого натра и немного воды. Плав постепенно растворился, образуя красно-коричневый непрозрачный раствор. Позднее к флуоресцеину, который остался на фильтре, я добавил щелочь и тоже перевел его в раствор. Растворы объединил.
(По большому счету отфильтровывать флуоресцеин было не обязательно: достаточно было максимально слить жидкость с осадка, а к образовавшейся суспензии добавить щелочь. Разумеется, кроме флуоресцеина в полученном растворе также содержится щелочь, сульфат натрия, фталат натрия и, возможно, остатки резорцина, но для дальнейших экспериментов это большого значения не имеет).
Каплю коричневого раствора добавил в трехлитровую банку с водой. Капля постепенно опускалась, образуя вихревые кольца, нити и "облака". Сначала капля была коричневой, потом постепенно стала желто-зеленой с отчетливой флуоресценцией. Неописуемая красота. Позже аналогичный эксперимент провел в пятилитровой банке.
Итак, приступим к экспериментам с флуоресцеином.
____________________________________________________________
Цель работы
Целью работы является проведение реакций окисления и конденсации для фенола и его производных.
Теоретическая часть
Фенолы – ароматические соединения, имеющие гидроксильные группы, непосредственно связанные с ароматическим ядром. По числу гидроксилов различают одноатомные, двухатомные и многоатомные фенолы. Простейший из них – оксибензол называют фенолом. Оксипроизводные толуола (метилфенолы) называют орто-, мета- и паракрезолами, а оксипроизводные ксилолов – ксиленолами. Фенолы ряда нафталина называют нафтолами. Простейшие двухатомные фенолы называются: о – диоксибензол – пирокатехин, м – диоксибензол – резорцин, n- диоксибензол – гидрохинон.
Многие фенолы легко окисляются, при этом часто образуется сложная смесь продуктов. В зависимости от окислителя и условий реакции можно получить различные продукты. Так, при парофазном окислении (t=540 0) о – ксилола получают фталевый ангидрид. Качественной реакцией на фенолы является проба с раствором хлорного железа, при этом образуется окрашенный ион. Фенол дает краснофиолетовую окраску, крезолы – голубую, другие фенолы – зеленую.
Реакция конденсации представляет собой внутримолекулярный или межмолекулярный процесс образования новой С-С-связи, обычно протекающий при участии конденсирующих реагентов, роль которых может быть самой различной: оказывает число каталитическое действие, давать промежуточные реакционноспособные продукты, просто связывать отщепляющуюся частицу, смещая равновесие в системе.
Реакция конденсации с отщеплением воды катализируется разнообразными реагентами: сильными кислотами,сильными щелочами (гидроокисями, алкоголятами, амидами, гидридами щелочных металлов, аммиаком, первичными и вторичными аминами).
Порядок выполнения работы
В данной работе проводится проверка возможности окисления фенолов и образования фталеинов реакцией конденсации.
3.1 Окисления фенола и нафтола
Окисление проводится раствором марганцево-кислого калия в присутствии раствора углекислого натра (соды).
3.1.1 оборудование и реактивы:
Пробирки;
Пипетки;
Фенол – водный раствор;
Нафтол - водный раствор;
Маргацевокислый калий (0,5 % - ный водный раствор);
Углекислый натрий (5 % - ный водный раствор);
3.1.2 Проведение опыта:
а) в пробирку поместить 1 мл водного раствора фенола или нафтола;
б) прилить 1 мл раствора углекислого натра (соды);
в) приливать по каплям раствор марганцевокислого калия при встряхивании пробирки. Наблюдать за измененим окраски раствора.
Окисление фенолов обычно протекает по различным направления и ведет к образованию сложной смеси веществ. Более легкая окисляемость фенолов, по сравнению с ароматическими углеводородами, обусловлена влиянием гидроксильной группы, резко повышающей подвижность атомов водорода при других атомах углерода бензольного яда.
3.2 Образование фталеинов.
3.2.1 Получение фенолфталеина.
Фенолфталеин образуется при реакции конденсации фенола со фталевым ангидридом в присутствии концентрированной серной кислоты.
Фталевый ангидрид вступает в конденсацию с фенолами, давая производные трифенилетана. Конденсация сопровождается отщеплением воды за счет кислорода одной из карбонильных групп ангидрида и подвижных атомов водорода бензольных ядер двух молекул фенола. Введение водоотнимающих средств, таких как концентрированная серная кислота, очень облегчает эту конденсацию.
Фенол образует фенолфталеин по следующей реакции:


 / \ /
/ \ /

 H H С
H H С
3.2.1.1 Оборудование и реактивы:
Пробирки;
Пипетки;
Электроплитка;
Фталевый ангидрид;
Серная кислота разбавленная 1:5;
3.2.1.2 Проведение опыта:
б) в эту же пробирку добавить примерно вдвое большее количество фенола;
в) встряхнуть несколько раз содержимое пробирки и осторожно добавить к нему 3-5 капель концентрированной серной кислоты, продолжая встряхивать;
г)нагреть пробирку на электроплитке до появления темно-красного окрашивания;
д) охладить пробирку и добавить в нее 5 мл воды;
е) к полученному раствору добавить по каплям раствор щелочи и наблюдать изменение окраски;
ж) после изменения окраски к содержимому пробирки добавить несколько капелл разбавленной серной кислоты до возвращения первоначальной окраски или до обесцвечивания.
3.2.2 Получение флуоресцеина.
Флуоресциин образуется при реакции конденсации резорцина с фталевым ангидридом в присутствии концентрированной серной кислоты.
Двухатомные фенолы с гидроксильными группами в мета – положении, вступая в конденсацию, выделяют две молекулы воды, одну за счет кислорода одной из карбонильных групп ангидрида и подвижных атомов водорода бензольных ядер двух молекул фенола. вторая молекула воды выделяется за счет гидроксильных групп двух молекул фенола с образованием шестичленного кольца.
Резорцин образует флуоресцеин по следующей реакции:
OH HO ОН HO OH


 / \ / \ /
/ \ / \ /

 H H С
H H С
3.2.1.1.Оборудование и реактивы:
Пробирки;
Пипетки;
Электроплитка;
Фталевый ангидрид;
Резорцин;
Серная кислота концентрированная;
Раствор едкого натрия(5-10 %-ный);
3.2.2.1 Проведение опыта:
а) взвесить 0.1-0.3 г фталевого ангидрида и поместить в пробирку;
б) в эту же пробирку добавить примерно вдвое большее количество резорцина и перемешать встряхивая;
в) к содержимому пробирки осторожно добавит 3-5 капель концентрированной серной кислоты;
г) смесь в пробирке нагреть до появления темно-красного окрашивания. Нагреть на электроплитке;
д) охладить содержимое пробирки и добавить в нее 5 мл воды;
е) в чистую пробирку внести 2-3 капли полученного раствора, добавить 1 мл раствора щелочи и разбавить большим количеством воды. Наблюдать за изменением окраски.
3.2.3 Образование аурина
Аурин получается при конденсации щавелевой кислоты с фенолом в присутствии серной кислоты.
При нагревании в присутствии серной кислоты щавелевая кислота конденсируется с тремя молекулами фенола, отщепляя воду и окись углерода с образованием аурина.
 |
|||
 |
|||
 H-O- - H H - -OH
H-O- - H H - -OH
 -H . OH O =
-H . OH O =
 | . С = O +3H 2 O+CO
| . С = O +3H 2 O+CO
 H - C
H - C
3.2.3.1. Оборудование и реактивы:
Пробирки;
Пипетки;
Щавелевая кислота;
Серная кислота концентрированная;
3.2.3.2 Проведение опыта:
а) взвесить 0,02-0,05г щавелевой кислоты и примерно вдвое больше фенола;
б) поместить оба реактива пробирку и перемешать встряхиванием;
в) добавить в пробирку 1-2 капли концентрированной серной кислоты;
г) осторожно нагреть пробирку со смесью до начала кипения и появления интенсивно желтой окраски;
д) охладить пробирку, добавить в нее 3-4 мл воды и встряхнуть. Наблюдать за появившейся окраской;
е) к полученному раствору добавить несколько капель раствора щелочи и наблюдать за изменением окраски;
3.3 Разложение мочевины (амида карбоминовой кислоты) при нагревании.
При нагревании выше температуры плавления мочевина распадается с выделением аммиака. При температуре 150 0 -160 0 С две молекулы мочевины отщепляют одну молекулу аммиака и дают хорошо растворимый в теплой воде биуреат:
H 2 N-OO-NH 2 +H-NH-OO-NH 2 H 2 N-CO-NH-CO-NH 2 +NH 3
Для биуреата характерно образование в щелочном растворе с солями меди ярко-красного комплексного соединения, имеющиге в растворе едкого натра следующий состав:
(NH 2 CO NH CONH 2) 2 *2NaOH*Cu(OH) 2
3.3.1 Оборудование и реактивы:
Пробирки;
Электроплитка;
Мочевина (карбомид);
Раствор едкого натрия(5-7 %-ный);
Раствор серной меди (1%-ный).
3.3.2 Проведение опыта:
а) взвесить 0,2-0,3г мочевины и поместить в сухую пробирку;
б) нагреть пробирку на электрической плитке;
в) наблюдать за происходящими изменениями: плавлением, выделением аммиака, затвердеванием;
г) охладить пробирку;
д) в охлажденную пробирку добавить 1-2мл теплой воды, взболтать и слить в другую пробирку;
е) к полученному мутному раствору добавить 3-4 капли раствора едкого натра до прозрачности. Затем добавить одну каплю раствора серной кислой меди и наблюдать изменение окраски (появляется красивое фиолетовое окрашивание).
Похожая информация.
Резорцин (Резорцинол, 1,3-дигидроксибензол) - мета-дигидроксибензол . Резорцин имеет специфический запах. Имеет тот же состав что и пирокатехин и гидрохинон , отличаясь от них лишь относительным расположением гидроксильных групп .
Физические свойства
Бесцветные кристаллы, до 70,8 °C существуют в α-модификации, выше в β-модификации. Легко растворим в этаноле , диэтиловом эфире , ацетоне , воде, труднорастворим в СНСl 3 , CS 2 , бензоле (в 100 г 2,2 г при 20 °C, 14,1 г при 60 °C).
Получение
Получают сульфированием бензола и затем щелочной плавкой (сплавлением 1,3-бензолдисульфокислоты с щелочью, в частности едким натром ). Что характерно: другие пара-замещённые бензолы, например, 1,4-бромфенол, 1,4-бензолсульфокислота при сплавлении со щёлочью дают резорцин.
Также его получают окислением 1,3-диизопропилбензола кислородом воздуха с последующим кислотным гидролизом образующегося бисгидропероксида до резорцина и ацетона .
Химические свойства
Резорцин обладает свойствами фенолов . Со щёлочами образует соли - феноляты, с диметилсульфатом даёт монометиловый эфир резорцина и диметиловый эфир резорцина . При взаимодействии с аммиаком образует 3-аминофенол. Взаимное влияние двух групп ОН обеспечивает легкость вступления резорцина в реакции электрофильного замещения главным образом в положения 4(6), труднее - в положение 2. Так при взаимодействии с галогенами образует 2,4,6-тригалогензамещенные. При действии азотной кислоты на резорцин образуется резазурин , при взаимодействии с концентрированной азотной кислотой (d=1.4 г/см 3) и концентрированной серной кислоты образуется 2,4,6-тринитрорезорцин . С пикриновой кислотой дает пикрат, т. пл. 89-90 °C.
Безопасность
Пыль и пары резорцина раздражают кожу и слизистые оболочки глаз и дыхательных путей, вызывают кашель.
Напишите отзыв о статье "Резорцин"
Примечания
Ссылки
- www.xumuk.ru/encyklopedia/2/3866.html
- www.abc-gid.ru/drugs/reestr/show/10708/
Отрывок, характеризующий Резорцин
– Что, барин, не спите? – сказал казак, сидевший под фурой.– Нет; а… Лихачев, кажется, тебя звать? Ведь я сейчас только приехал. Мы ездили к французам. – И Петя подробно рассказал казаку не только свою поездку, но и то, почему он ездил и почему он считает, что лучше рисковать своей жизнью, чем делать наобум Лазаря.
– Что же, соснули бы, – сказал казак.
– Нет, я привык, – отвечал Петя. – А что, у вас кремни в пистолетах не обились? Я привез с собою. Не нужно ли? Ты возьми.
Казак высунулся из под фуры, чтобы поближе рассмотреть Петю.
– Оттого, что я привык все делать аккуратно, – сказал Петя. – Иные так, кое как, не приготовятся, потом и жалеют. Я так не люблю.
– Это точно, – сказал казак.
– Да еще вот что, пожалуйста, голубчик, наточи мне саблю; затупи… (но Петя боялся солгать) она никогда отточена не была. Можно это сделать?
– Отчего ж, можно.
Лихачев встал, порылся в вьюках, и Петя скоро услыхал воинственный звук стали о брусок. Он влез на фуру и сел на край ее. Казак под фурой точил саблю.
– А что же, спят молодцы? – сказал Петя.
– Кто спит, а кто так вот.
– Ну, а мальчик что?
– Весенний то? Он там, в сенцах, завалился. Со страху спится. Уж рад то был.
Долго после этого Петя молчал, прислушиваясь к звукам. В темноте послышались шаги и показалась черная фигура.
– Что точишь? – спросил человек, подходя к фуре.
– А вот барину наточить саблю.
– Хорошее дело, – сказал человек, который показался Пете гусаром. – У вас, что ли, чашка осталась?
– А вон у колеса.
Гусар взял чашку.
– Небось скоро свет, – проговорил он, зевая, и прошел куда то.
Петя должен бы был знать, что он в лесу, в партии Денисова, в версте от дороги, что он сидит на фуре, отбитой у французов, около которой привязаны лошади, что под ним сидит казак Лихачев и натачивает ему саблю, что большое черное пятно направо – караулка, и красное яркое пятно внизу налево – догоравший костер, что человек, приходивший за чашкой, – гусар, который хотел пить; но он ничего не знал и не хотел знать этого. Он был в волшебном царстве, в котором ничего не было похожего на действительность. Большое черное пятно, может быть, точно была караулка, а может быть, была пещера, которая вела в самую глубь земли. Красное пятно, может быть, был огонь, а может быть – глаз огромного чудовища. Может быть, он точно сидит теперь на фуре, а очень может быть, что он сидит не на фуре, а на страшно высокой башне, с которой ежели упасть, то лететь бы до земли целый день, целый месяц – все лететь и никогда не долетишь. Может быть, что под фурой сидит просто казак Лихачев, а очень может быть, что это – самый добрый, храбрый, самый чудесный, самый превосходный человек на свете, которого никто не знает. Может быть, это точно проходил гусар за водой и пошел в лощину, а может быть, он только что исчез из виду и совсем исчез, и его не было.
Что бы ни увидал теперь Петя, ничто бы не удивило его. Он был в волшебном царстве, в котором все было возможно.
Он поглядел на небо. И небо было такое же волшебное, как и земля. На небе расчищало, и над вершинами дерев быстро бежали облака, как будто открывая звезды. Иногда казалось, что на небе расчищало и показывалось черное, чистое небо. Иногда казалось, что эти черные пятна были тучки. Иногда казалось, что небо высоко, высоко поднимается над головой; иногда небо спускалось совсем, так что рукой можно было достать его.
Петя стал закрывать глаза и покачиваться.
Капли капали. Шел тихий говор. Лошади заржали и подрались. Храпел кто то.
– Ожиг, жиг, ожиг, жиг… – свистела натачиваемая сабля. И вдруг Петя услыхал стройный хор музыки, игравшей какой то неизвестный, торжественно сладкий гимн. Петя был музыкален, так же как Наташа, и больше Николая, но он никогда не учился музыке, не думал о музыке, и потому мотивы, неожиданно приходившие ему в голову, были для него особенно новы и привлекательны. Музыка играла все слышнее и слышнее. Напев разрастался, переходил из одного инструмента в другой. Происходило то, что называется фугой, хотя Петя не имел ни малейшего понятия о том, что такое фуга. Каждый инструмент, то похожий на скрипку, то на трубы – но лучше и чище, чем скрипки и трубы, – каждый инструмент играл свое и, не доиграв еще мотива, сливался с другим, начинавшим почти то же, и с третьим, и с четвертым, и все они сливались в одно и опять разбегались, и опять сливались то в торжественно церковное, то в ярко блестящее и победное.
«Ах, да, ведь это я во сне, – качнувшись наперед, сказал себе Петя. – Это у меня в ушах. А может быть, это моя музыка. Ну, опять. Валяй моя музыка! Ну!..»
Он закрыл глаза. И с разных сторон, как будто издалека, затрепетали звуки, стали слаживаться, разбегаться, сливаться, и опять все соединилось в тот же сладкий и торжественный гимн. «Ах, это прелесть что такое! Сколько хочу и как хочу», – сказал себе Петя. Он попробовал руководить этим огромным хором инструментов.
«Ну, тише, тише, замирайте теперь. – И звуки слушались его. – Ну, теперь полнее, веселее. Еще, еще радостнее. – И из неизвестной глубины поднимались усиливающиеся, торжественные звуки. – Ну, голоса, приставайте!» – приказал Петя. И сначала издалека послышались голоса мужские, потом женские. Голоса росли, росли в равномерном торжественном усилии. Пете страшно и радостно было внимать их необычайной красоте.
Фенолы могут реагировать как по гидроксильной группе, так и по бензольному кольцу.
1. Реакции по гидроксильной группе
Углерод-кислородная связь в фенолах гораздо прочнее, чем в спиртах. Например, фенол не может быть превращен в бромбензол действием на него бромоводорода, тогда как циклогексанол при нагревании с бромоводородом легко превращается в бромциклогексан:
Как и алкоксиды феноксиды реагируют с алкилгалогенидами и другими алкилирующими реагентами с образованием смешанных эфиров:
 (23)
(23)
Фенетол
 (24)
(24)
Анизол
Алкилирование фенолов галогенуглеводородами или диметилсульфатом в щелочной среде представляет собой модификацию реакции Вильямсона. По реакции алкилирования фенолов хлоруксусной кислотой получают такие гербициды как 2,4-дихлорфеноксиуксусная кислота (2,4-Д).
 (25)
(25)
2,4-Дихлорфеноксиуксусная кислота (2,4-Д)
и 2,4,5-трихлорфеноксиуксусная кислота (2,4,5-Т).
 (26)
(26)
2,4,5-трихлорфеноксиуксусная кислота (2,4,5-Т)
Исходный 2,4,5-трихлорфенол получают по схеме:
 (27)
(27)
1,2,4,5- Тетрахлорфенол 2,4,5-трихлорфеноксид натрия 2,4,5-трихлорфенол
При перегреве на стадии получения 2,4,5-трихлорфенола вместо него может образовываться очень токсичный 2,3,7,8-тетрахлордибензодиоксин:
2,3,7,8-Тетрахлордибензодиоксин
Фенолы являются более слабыми нуклеофилами, чем спирты. По этой причи-не они в отличие от спиртов не вступают в реакцию этерификации. Для получения сложных эфиров фенолов используют хлорангидриды и ангидриды кислот:
Фенилацетат
Дифенилкарбонат
Упр.17. Тимол (3-гидрокси-4-изопропилтолуол) содержится в тимьяне и используется в качестве антисептика средней силы в зубных пастах и жидкостях для полоскания рта. Его получают алкилированием по Фриделю – Крафтсу
м -крезола 2-пропанолом в присутствии серной кислоты. Напишите эту реакцию.
2. Замещение в кольцо
Оксигруппа фенола очень сильно активирует ароматическое кольцо по отношению к реакциям электрофильного замещения. В качестве промежуточных соединений вероятнее всего образуются оксониевые ионы:


При проведении реакции электрофильного замещения в случае фенолов необходимо применять специальные меры для того, чтобы предотвратить полизамещение и окисление.
3. Нитрование
Фенол нитруется гораздо легче бензола. При действии на него концентриро-ванной азотной кислоты образуется 2,4,6-тринитрофенол (пикриновая кислота):

Пикриновая кислота
Наличие в ядре трех нитрогрупп резко увеличивает кислотность фенольной группы. Пикриновая кислота является, в отличие от фенола, уже довольно сильной кислотой. Наличие трех нитрогрупп делает пикриновую кислоту взрывчатой, она используется для приготовления мелинита. Для получения мононитрофенолов необходимо использовать разбавленную азотную кислоту и проводить реакцию при низких температурах:

Получается смесь о- и п- нитрофенолов с преобладанием о- изомера. Эта смесь легко разделяется благодаря тому, что только о- изомер обладает летучестью с водяным паром. Большая летучесть о- нитрофенола объясняется образованием внутримолекулярной водородной связи, в то время как в случае
п- нитрофенола возникает межмолекулярная водородная связь.

4. Сульфирование
Сульфирование фенола осуществляется очень легко и приводит к образованию в зависимости от температуры преимущественно орто - или пара -фенолсульфокислот:

5. Галогенирование
Высокая реакционная способность фенола приводит к тому, что даже при его обработке бромной водой происходит замещение трех атомов водорода:
 (31)
(31)
Для получения монобромфенола необходимо принимать специальные меры.
 (32)
(32)
п -Бромфенол
Упр.18. На 0.94 г фенола действуют небольшим избытком бромной воды. Какой продукт и в каком количестве при этом образуется?
6. Реакция Кольбе
Диоксид углерода присоединяется к феноксиду натрия по реакции Кольбе, представляющей собой реакцию электрофильного замещения, в которой электрофилом является диоксид углерода
 (33)
(33)
Фенол Феноксид натрия Салицилат натрия Салициловая кислота
Механизм:
 (М 5)
(М 5)
Действием на салициловую кислоту уксусного ангидрида получают аспирин:
 (34)
(34)
Ацетилсалициловая кислота
Если оба орто -положения заняты, то замещение проходит по пара- положению:
 (35)
(35)
Реакция проходит по следующему механизму:
 (М 6)
(М 6)

7. Конденсация с карбонилсожержащими соединениями
При нагревании фенола с формальдегидом в присутствии кислоты образуется фенолформальдегидная смола:
 (36)
(36)
Фенолформальдегидная смола
Конденсацией фенола с ацетоном в кислой среде получают 2,2-ди(4-гидроксифенил)пропан, получивший промышленное название бисфенол А:
Бисфенол А
2,2-ди(4-гидроксифенил)пропан
ди(4-оксифенил)диметилметан
Обработкой бисфенола А фосгеном в пиридине получают лексан:
В парисутствии серной кислоты или хлорида цинка фенол конденсируется с фталевым ангидридом с образованием фенолфталеина:
 (39)
(39)
Фталевый ангидрид Фенолфталеин
При сплавлении фталевого ангидрида с резорцином в присутствии хлорида цинка происходит аналогичная реакция и образуется флуоресцеин:
 (40)
(40)
Резорцин Флуоресцеин
Упр.19. Изобразите схему конденсации фенола с формальдегидом. Какое практическое значение имеет эта реакция?
8. Перегруппировка Кляйзена
Фенолы вступают в реакции алкилирования по Фриделю-Крафтсу. Например, при взаимодействии фенола с аллилбромидом в присутствии хлорида алюминия образуется 2-аллилфенол:
 (41)
(41)
Этот же продукт образуется и при нагревании аллилфенилового эфира в результате внутримолекулярной реакции называемой перегруппировкой Кляйзена:
 |
 |
Аллилфениловый эфир 2-Аллилфенол
Реакция
 (43)
(43)
Проходит по следующему механизму:
 (44)
(44)
Перегруппировка Кляйзена происходит также и при нагревании аллилвинилового эфира или 3,3-диметил-1,5-гексадиена:
 (45)
(45)
Аллилвиниловый эфир 4-Пентеналь
 (46)
(46)
3,3-Диметил- 2-Метил-2,6-
1,5-гексадиен гексадиен
Известны и другие реакции этого типа, например, Реакция Дильса-Альдера. Их называют перициклическими реакциями.
Фталевый ангидрид Фенолфталеин
При сплавлении фталевого ангидрида с резорцином в присутствии хлорида цинка происходит аналогичная реакция и образуется флуоресцеин:
Резорцин Флуоресцеин
3.8 Перегруппировка Кляйзена
Фенолы вступают в реакции алкилирования по Фриделю-Крафтсу. Например, при взаимодействии ф
енола с аллилбромидом в присутствии хлорида алюминия образуется 2-аллилфенол:
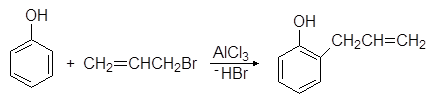
Этот же продукт образуется и при нагревании аллилфенилового эфира в результате внутримолекулярной реакции называемой перегруппировкой Кляйзена:
 |
|||
 |
|||
Аллилфениловый эфир 2-Аллилфенол
Реакция:

Проходит по следующему механизму:

Перегруппировка Кляйзена происходит также и при нагревании аллилвинилового эфира или 3,3 – диметил – 1,5 – гексадиена: AAAAAAAAAAAAAAAAAAAAAAAAAAA

3.9 Поликонденсация
Поликонденсация фенола с формальдегидом (по этой реакции происходит образование фенолформальдегидной смолы:

3.10 Окисление
Фенолы легко окисляются даже под действием кислорода воздуха. Так, при стоянии на воздухе фенол постепенно окрашивается в розовато-красный цвет. При энергичном окислении фенола хромовой смесью основным продуктом окисления является хинон. Двухатомные фенолы окисляются еще легче. При окислении гидрохинона образуется хинон.
3.11 Кислотные свойства
Кислотные свойства фенола проявляются в реакциях со щелочами (сохранилось старинное название «карболовая кислота»):
С6Н5ОН + NaOH <-> C6H5ONa + Н2O
Фенол, однако, является очень слабой кислотой. При пропускании через раствор фенолятов углекислого или сернистого газов выделяется фенол – такая реакция позывает, что фенол – более слабая кислота, чем угольная и сернистая:
C6H5ONa + СO2 + Н2O -> С6Н5ОН + NaHCО3
Кислотные свойства фенолов ослабляются при введении в кольцо заместителей I рода и усиливаются при введении заместителей II рода.
4. Способы получения
Производство фенола в промышленном масштабе осуществляется тремя способами:
– Кумольный метод. Этим способом получают более 95% всего производимиого в мире фенола. В каскаде барботажных колонн кумол подвергают некаталитическому окислению воздухом с образованием гидропероксида кумола (ГПК). Полученный ГПК, при катализе серной кислотой, разлагают с образованием фенола и ацетона. Кроме того, ценным побочным продуктом этого процесса является α-метилстирол.
– Около 3% всего фенола получают окислением толуола, с промежуточным образованием бензойной кислоты.
– Весь остальной фенол выделяют из каменноугольной смолы.
4.1 Окислением кумола
Фенолы выделяют из каменноугольной смолы, а также из продуктов пиролиза бурых углей и древесины (деготь). Промышленный способ получения самого фенола С6Н5ОН основан на окислении ароматического углеводорода кумола (изопропилбензол) кислородом воздуха с последующим разложением получающейся гидроперекиси, разбавленной H2SO4. Реакция проходит с высоким выходом и привлекательна тем, что позволяет получить сразу два технически ценных продукта – фенол и ацетон. Другой способ–каталитический гидролиз галогензамещенных бензолов.

4.2 Получение из галогенбензолов
При нагревании хлорбензола и гидроксида натрия под давлением получают фенолят натрия, при дальнейшей обработке которого кислотой образуется фенол:
С6Н5-CI + 2NaOH -> С6Н5-ONa + NaCl + Н2O
4.3 Получение из ароматических сульфокислот
Реакция проводится при сплавлении сульфокислот с щелочами. Первоначально образующиеся феноксиды обрабатывают сильными кислотами для получения свободных фенолов. Метод обычно применяют для получения многоатомных фенолов:

4.4 Получение из хлорбензола
Известно, что атом хлора прочно связан с бензольным кольцом, поэтому реакцию замены хлора на гидроксильную группу проводят в жестких условиях (300 °С, давление 200 МПа):
C6H5-Cl + NaOH – > C6H5-OH + NaCl
5. Применение фенолов
Раствор фенола используют в качестве дезинфицирующего средства (карболовая кислота). Двухатомные фенолы – пирокатехин, резорцин (рис. 3), а также гидрохинон (пара-дигидроксибензол) применяют как антисептики (антибактериальные обеззараживающие вещества), вводят в состав дубителей для кожи и меха, как стабилизаторы смазочных масел и резины, а также для обработки фотоматериалов и как реагенты в аналитической химии.
В виде отдельных соединений фенолы используются ограниченно, зато их различные производные применяют широко. Фенолы служат исходными соединениями для получения разнообразных полимерных продуктов – феноло-альдегидных смол, полиамидов, полиэпоксидов. На основе фенолов получают многочисленные лекарственные препараты, например, аспирин, салол, фенолфталеин, кроме того, красители, парфюмерные продукты, пластификаторы для полимеров и средства защиты растений.
Мировое потребление фенола имеет следующую структуру:
· 44% фенола расходуется на производство бисфенола А, который, в свою очередь, используется для производства поликарбона и эпоксидных смол;
· 30% фенола расходуется на производство фенолформальдегидных смол;
· 12% фенола гидрированием превращается в циклогексанол, используемый для получения искусственных волокон – нейлона и капрона;
· остальные 14% расходуются на другие нужды, в том числе на производство антиоксидантов (ионол), неионогенных ПАВ – полиоксиэтилированных алкилфенолов (неонолы), других фенолов (крезолов), лекарственных препаратов (аспирин), антисептиков (ксероформа) и пестицидов.
· 1,4% фенола применяется в медицине (орасепт), как обезболивающее и антисептическое средство.
6. Токсические свойства
Фенол ядовит. Вызывает нарушение функций нервной системы. Пыль, пары и раствор фенола раздражают слизистые оболочки глаз, дыхательных путей, кожу (ПДК 5 мг/м³, в водоёмах 0,001 мг/л).
